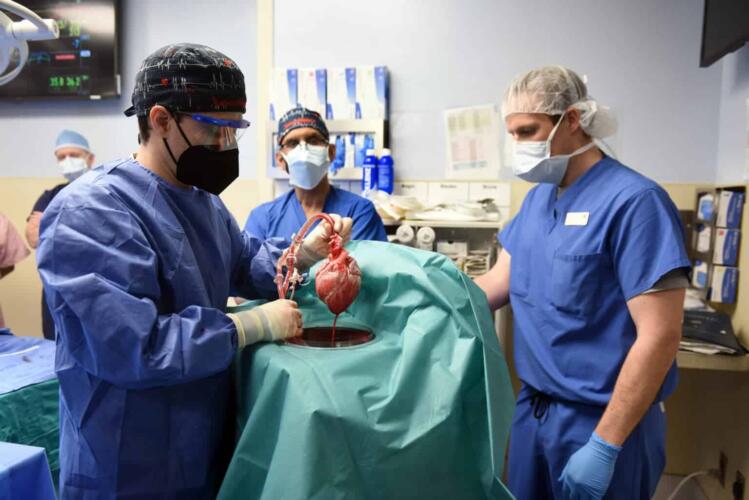
في 7 يناير/كانون الثاني 2022، دخل “ديفيد بينيت” إلى غرفة العمليات في مركز جامعة ميريلاند الطبي للخضوع إلى عملية جراحية لم يُنجز مثلها من قبل على إنسان. دخل بينيت، والذي يبلغ من العمر 57 سنة، المستشفى، وكان طريح الفراش لشهور بسبب إصابته بحالة مهددة للحياة من عدم انتظام دقات القلب. قلبه كان يفشل، وكان بحاجة إلى قلب جديد.
لم يكن بينيت يستجيب للعلاجات التقليدية، كما أنه لم يكن مؤهلاً للخضوع إلى عملية زرع قلب بشري أو مضخة قلبية. مع ذلك، كان لدى العلماء والأطباء في مركز بالتيمور الطبي خياراً آخراً خطيراً: إجراء عملية زرع قلب خنزير معدّل وراثياً.
قال بينيت للجراحين في مركز جامعة ميريلاند الطبي قبل الخضوع للعملية بيوم: “إما أن أموت أو أن أخضع لعملية الزرع هذه”، وأضاف: أريد أن أعيش. اعلم أن فرصي قليلة، ولك هذا هو خياري الوحيد”.
نجاح أول عملية زرع قلب خنزير في جسم إنسان
أبلغ فريق الأطباء في 10 يناير/كانون الثاني 2022 أنهم أكملوا العملية الجراحية التي استغرقت 8 ساعات، ما يجعل بينيت أول شخص يتلقى قلب خنزير بنجاح. قال “بارتلي غريفيث”، الطبيب ومدير برنامج زرع القلب في مركز جامعة ميريلاند الطبي، والذي قاد فريق عملية الزرع، لصحيفة “ذا نيويورك تايمز“: “القلب يعمل ويبدو أنه طبيعي. نحن نشعر بسعادة غامرة، لكن لا نعلم ما يخبّئه المستقبل”.
وعلى الرغم من أنه قد مر على العملية أيام فقط، إلا أن الأطباء يقولون إن قلب بينيت الجديد يؤدي وظائفه حتى الآن كما هو متوقّع، وأن جسمه لم يرفض العضو الجديد. لا يزال الأطباء يراقبون حالة بينيت عن كثب.
يقول “روبرت مونتغمري“، طبيب مختص في عمليات زرع الأعضاء ومدير معهد “لانغون” لزرع الأعضاء التابع لجامعة نيويورك، والذي لم يشارك في عملية بينيت: “أعتقد أن هذا الإنجاز مثير للغاية”. كانت نتائج العملية مهمة أيضاً بالنسبة لمونتغمري، إذ أنه خضع لعملية زرع قلب في 2018 بسبب إصابته بمرض وراثي قد يؤثّر في المستقبل على أعضاء آخرين في عائلته. يضيف مونتغمري: “لا يزال الوقت مبكراً، لكن يبدو أن القلب يؤدي وظائفه، وهذا أمر استثنائي بحد ذاته”.
اقرأ أيضاً: طريقة جديدة تكشف احتمالية الإصابة بأمراض القلب قبل 20 عاماً
موافقة طارئة من قبل إدارة الغذاء والدواء الأميركية على العملية
لم تتم الموافقة بعد على إجراء عمليات زرع قلوب الخنازير من قبل إدارة الغذاء والدواء الأميركية، لكن منحت هذه الوكالة موافقة طارئة لعملية بينيت في 31 ديسمبر/كانون الأول 2021. أُجريت هذه العملية التجريبية في وقت تزداد فيه الحاجة لإجراء عمليات زرع الأعضاء في البلاد، إذ تحتوي قائمة انتظار عمليات زرع الأعضاء على أكثر من 100 ألف مريض، ويموت نحو 17 مريضاً يومياً منهم، وذلك وفقاً لأحدث البيانات من موقع “أورغن دونر” التابع للحكومة الفدرالية. يتجاوز الطلب على الأعضاء عدد المتبرعين المتوفّرين بقدر كبير.
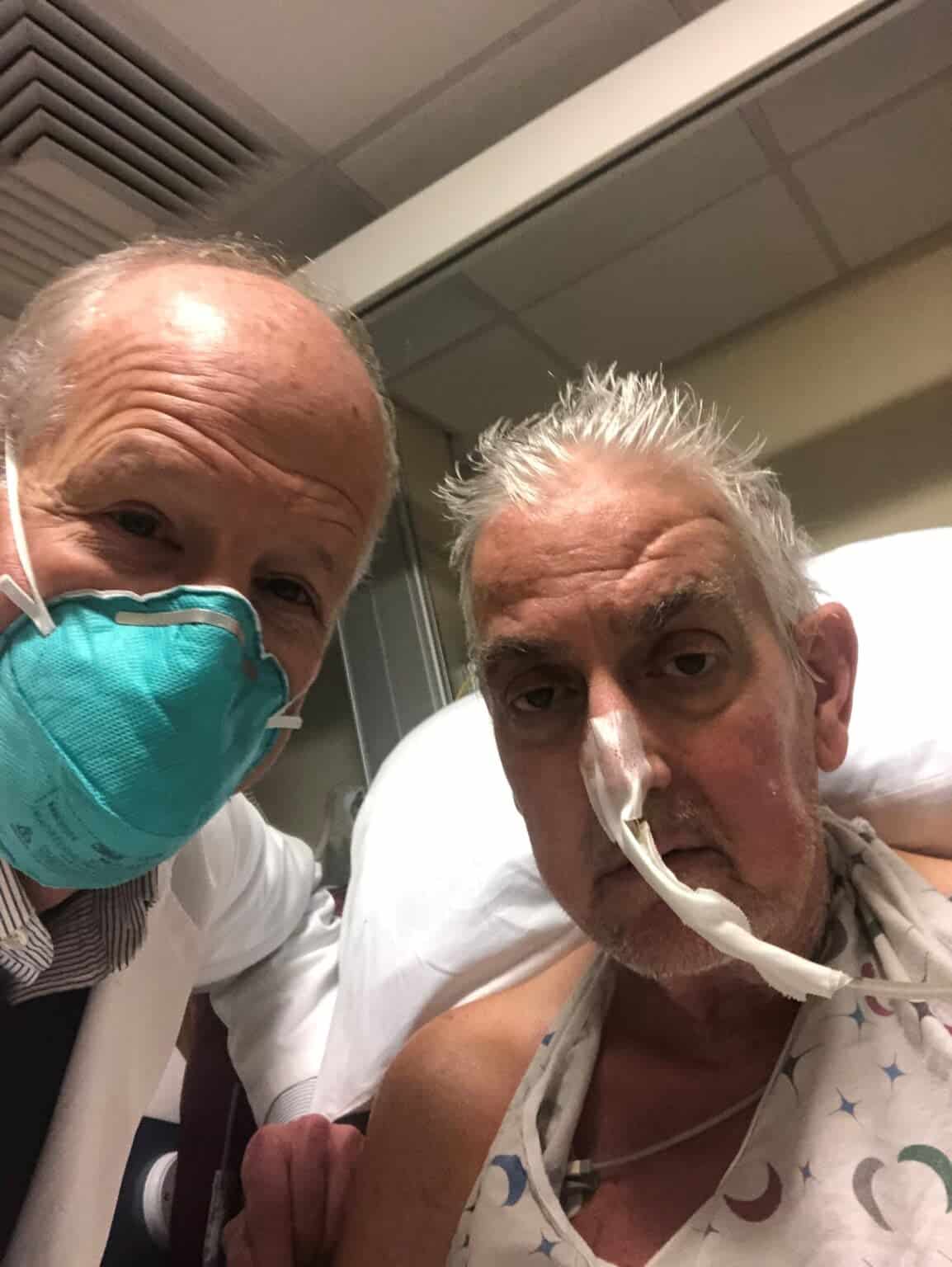
يقول مونتغمري: “ببساطة، لا يوجد ما يكفي من الأعضاء”. كان مونتغمري واحداً من فريق من الأطباء الذين نجحوا في زرع كلية خنزير معدّل وراثياً في جسم إنسان في 2021، ويشير إلى أنه من بين 800 ألف مريض يخضعون لعملية غسيل الكلى، ويعانون من أمراض كلوية في مراحلها المتقدمة، يوجد منهم 90 ألفاً على قوائم انتظار زرع الأعضاء. توفر عمليات زرع أعضاء الخنازير “طريقة مختلفة محتملة لملء الفجوة بين العرض والطلب”، حسب تعبير مونتغمري.
تطوّر المجال البحثي لعمليات زراعة الأعضاء الحيوانية في البشر وتقنياته قبل تحقيق هذا الإنجاز الأخير بزمنٍ طويل، من سيطرة الخرافات والعلم الزائف إلى التطبيقات الطبية المتقدمة. يقول مونتغمري إن هذا المجال، والذي يسمى “نقل الأعضاء بين الكائنات الحية”، له تاريخ طويل، وهو قد عمل فيه لأكثر من 30 عاماً.
يقول مونتغمري: “أُخذت فكرة نقل الأعضاء بين الكائنات الحية بعين الاعتبار منذ نشوء مجال زراعة الأعضاء”، ويضيف: “فكّر البشر باستخدام أعضاء الحيوانات لأكثر من 100 سنة”.
طوال القرن التاسع عشر، استخدم الدجاج والضفادع والكلاب والجرذان وغيرها من الحيوانات في عمليات ترقيع الجلد. استمر الباحثون في هذا المجال بمواجهة مشاكل عدم التوافق بين أعضاء ونُسُج البشر والحيوانات، ويعود هذا إلى أن أجسام العديد من الحيوانات تحتوي على سكر نُسُج خلوية يدعى “غالاكتوز ألفا-1، 3-غالاكتوز“، والذي يشار إليه عادة باسم”ألفا-غال”. يقول مونتغمري: “يوجد هذا السكر على أسطح البكتيريا أيضاً”. يتعرّض البشر لهذه البكتيريا منذ الولادة في الجهاز الهضمي، ما يحفّز الجهاز المناعي على تركيب أجسام مضادة خاصة بسكّر ألفا-غال لمنع هذه البكتيريا من الدخول إلى مجرى الدم. يقول مونتغمري: “تحتوي أجسام البشر على مخزون كبير من هذه الأجسام المضادة التي توجد في الدم”، وتهاجم هذه الأجسام الأعضاء الحيوانية المزروعة لأنها تتحسس وجود سكر ألفا-غال.
في ستينيّات القرن الماضي، بدأ الأطباء الجراحون في البحث في الحيوانات الأقرب وراثياً إلى البشر: الرئيسيات. يقول مونتغمري: “الرئيسيات أقرب بكثير إلى البشر على المقياس التطوري، لذلك لا توجد مشكلة عدم التوافق المباشرة مع سكر ألفا-غال عند بعض أنواع الرئيسيات”. قام جرّاح في جامعة تولين في ولاية نيو أورلينز بزرع كلى من قرود الشمبانزي في أجسام مرضاه، وظل واحد منهم على قيد الحياة لـ 9 أشهر، وتلقّت الرضيعة الشهيرة “بيبي فاي“، وهي كانت مولودة حديثة تعاني من ضعف نمو القلب، قلب قرد بابون، لكن رفضه جسمها بعد 20 يوماً.
اقرأ أيضاً: دراسةٌ تُظهر تأثير تسارع نبضات القلب على اتخاذ القرارات
أخلاقيات نقل الأعضاء بين الكائنات الحية
غدت فكرة نقل الأعضاء من الرئيسيات مثيرة للجدل بحلول تسعينيات القرن الماضي. يقول مونتغمري: “هذه الحيوانات أصبحت أكثر ندرة بكثير في الأرض”، ويضيف: “حضرت مؤتمراً حول نقل الأعضاء بين الكائنات الحية في تسعينيات القرن الماضي، وكانت ‘جين غودال’ هي المتحدّثة الرئيسية … في نهاية المؤتمر، كان واضحاً تماماً للجميع أن الرئيسيات لن تكون الكائنات المتبرعة بالأعضاء التي نرغب باستخدامها”. يضيف مونتغمري أن المخاوف من نقل الأمراض ذات المنشأ الحيواني إلى البشر كانت في ازدياد أيضاً، غالباً بسبب جائحة الإيدز.
أصبحت الظروف مناسبة للاستعانة بالخنازير، إذ أنها أصبحت المتبرعات الرئيسية للأعضاء نظراً لوفرتها وكبر أحجام صغارها وسهولة إكثارها ونموها السريع، وتقارب أحجام أعضائها مع أحجام أعضاء البشر بشكل عام.
بالإضافة إلى ذلك، يقول مونتغمري إن أغلبية البشر لديهم علاقة مختلفة مع هذه الحيوانات كمصدر للغذاء، إلا أنه يتوقع أن المخاوف الأخلاقية ستستمر بالازدياد مع تطوّر هذا المجال، مثل ما إذا يجب أن تُعدّل الحيوانات وراثياً بهدف زراعة الأعضاء أم لا.
اقرأ أيضاً: من الكلى إلى القلب: هذا ما يجب أن تعرفه عن زراعة الأعضاء
تحديات نقل الأعضاء بين الكائنات الحية
كانت هناك عقبتان كبيرتان يتعين على مجال البحث في نقل الأعضاء بين الكائنات الحية تجاوزهما قبل أن تصبح الخنازير خياراً قابلاً للتطبيق: المشكلات المتعلقة بسكّر ألفا-غال والانتقال المحتمل للفيروسات، ولا سيما “الفيروس الارتجاعي الداخلي الخنزيري”، والذي اكتُشف في عام 1997. حالياً، تمكّن الباحثون من إزالة سكّر ألفا-غال من جينوم الخنازير بالتعديل الوراثي. اليوم، خضع الكثيرون لعلاج الحروق باستخدام جلد الخنزير، أو لزراعة صمامات قلب خنزير، أو تلقوا خلايا خنزير، مثل تلك التي تساعد على إنتاج الأنسولين، ولم يتعرضوا لأي أمراض.
يقول مونتغمري: “أصبح التعديل الوراثي أمراً سهلاً للغاية، خاصة الآن باستخدام تقنية ‘كريسبر’“. يضيف مونتغمري أن ما يقرب من 200 شخصاً قد تلقوا خلايا خنازير وخلايا جذعية وأنسجة خنازير وترقيعاً جلديّاً دون التعرض للأمراض الحيوانية المنشأ.
يتم إكثار الخنازير المعدلة وراثياً المستخدمة للتبرع بالأعضاء ودراستها ورعايتها في منشآت نظيفة للغاية، كما يتم فحصها بحثاً عن العوامل الممرضة المحتملة. يقول مونتغمري: “تشبه هذه الأماكن غرف العمليات”، ويضيف: “وتُعامل الخنازير فيها معاملة إنسانية للغاية”.
حتى الآن، أُجريت معظم عمليات الزرع التجريبية بين الخنازير والحيوانات الأخرى فقط. يقول مونتغمري عن عملية الزرع الأخيرة التي أجريت في المركز الطبي التابع لجامعة ميريلاند: “تتمثّل القفزة النوعية في تطبيق هذه العمليات على البشر”، ويضيف: “لقد تم إنجاز الأمر بالفعل، والآن، يجب علينا أن نفهم تبعاته على البشر، وأن نبدأ في العمل على تحسين النتائج. لكننا بحاجة لأن نسرع، دعونا نمضي قدماً بجرأة”.
