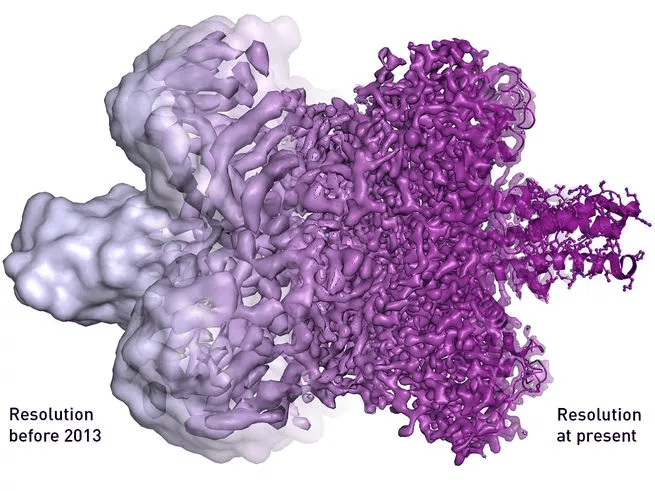
قبل اختراع طريقة الفحص المجهري الإلكتروني فائق البرودة، والتي نال بها علماء الكيمياء الحيوية: جاك دوبوشيه، ويواكيم فرانك، وريتشارد هينديرسون جائزة نوبل للكيمياء، في الرابع من أكتوبر عام 2017، كان يجب على العلماء أن يصبغوا أو يثبتوا الخلايا قبل أن يفحصوها تحت المجهر الإلكتروني. وكانت تلك العملية تسبب غالباً انفصال البنى الحيوية الهشة، وإذا لم يفعلوا ذلك ، فإن الإشعاع القادم من المجهر الإلكتروني أو من الفراغ الذي يضع العلماء الخلايا فيه، يحول العينات الحية إلى ما يشبه العصيدة. وتسمح المعالجة الإلكترونية فائق البرودة للعلماء بفحص الخلايا كما لو أنها كانت في بيئتها السائلة الحقيقية، تماماً كما لو كانت في أجسامناً.
يقول أليسون كامبيل، رئيس الجمعية الكيميائية الأميركية: "حتى نفهم جيداً كيف تعمل هذه البروتينات وتؤدي وظائفها، فإن النظر إلى حالتها في البيئة السائلة أمر بالغ الأهمية".
في عام 1975، نظّر يواكيم فرانك، من وزارة الصحة في ولاية نيويورك، لعملية يمكن فيها دمج المعلومات التي كانت محدودة في ذلك الوقت، والتي يقدمها المجهر الإلكتروني، في صورة عالية الدقة، ثلاثية الأبعاد، وأمضى أكثر من عقد من الزمن في وضع خوارزميات لهذا البرنامج، والتي جعلت الفحص المجهري الإلكتروني فائق البرودة ممكناً.
ثم في عام 1984، نشر فريق بقيادة جاك دوبوشيه دراسة عن استخدام المجهر الإلكتروني في تصوير الفيروس الذي غالباً ما يسبب نزلات البرد، والحفاظ عليه في طبقة رقيقة من الماء المبرد بسرعة، بحيث يصبح أقرب إلى الزجاج منه إلى الجليد. وجاء في هذه الدراسة: "تظهر الجسيمات الفيروسية خالية من الضرر الناجم عن الجفاف أو التجميد أو الامتزاز الذي يحدث كنوع من الدعم في إعداد العينات الحيوية للفحص المجهري الإلكتروني التقليدي. وتقدم العينات المزجّجة في الفحص المجهري الإلكتروني فائق البرودة إمكانية المراقبة عالية الدقة، والتي تجعلها أفضل مقارنةً بأي طريقة فحص مجهري إلكتروني أخرى".
وفي عام 1991، نشر ريتشارد هينديرسون أول صورة لبروتين بكتيري بدقة عالية كافية لإظهار كل ذرة مفردة.
ومنذ ذلك الحين، استخدم العلماء المجهر الإلكتروني فائق البرودة لفحص أكثر من 100 جزيء: البروتينات التي تسبب الطعم الحار للفلفل على الفم، وخلايا زيكا، واللويحات المرتبطة بمرض ألزهايمر، والبروتينات التي تسبب مقاومة المضادات الحيوية، وهذه مجرد أمثلة. ويساعد الحصول على صورة أكثر وضوحاً وأعلى دقة لهذه البروتينات العلماء على تطوير أدوية جديدة وغيرها من العلاجات لمكافحة الأمراض التي تسببها. يقول كامبل: "كنت أتمنى لو كنا نملك هذه الإمكانيات عندما كنت لا أزال نشطاً في مجال البحث". ويضيف: "إن جميع الإمكانيات لم تُدرك بعد".