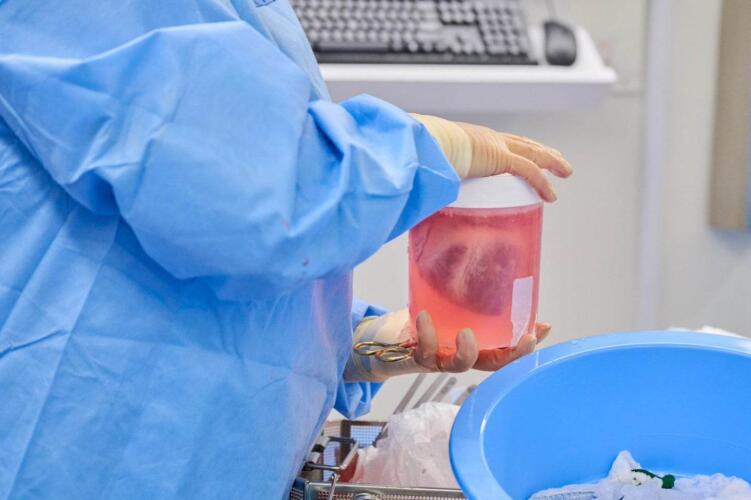
وفقاً للمنظمة غير الربحية التي تدير عمليات زرع الأعضاء في الولايات المتحدة، يوجد أكثر من 100 ألف أميركي الآن في قوائم الانتظار الخاصة بالحصول على الأعضاء، ويموت 17 شخصاً منهم يومياً. يمكن لإنشاء إمداد جدير بالاعتماد من أعضاء الخنازير أن يخفف من هذه الضائقة. ويبدو أن التكنولوجيا التي يتطلبها هذا الأمر أصبحت في متناول اليد أخيراً.
بعد عقد من إجراء الأبحاث، تم إحراز تقدّم ملحوظ في مجال نقل الأعضاء بين الكائنات الحية خلال السنة الفائتة. في يناير/كانون الثاني 2022، نجح جراحون من جامعة ألاباما في مدينة برمنغهام في إنجلترا بزرع كلى الخنازير في مريضين يعانيان من الموت الدماغي. وفي الشهر نفسه، قام فريق من جامعة ميريلاند بزرع قلب خنزير في جسم مريض اسمه ديفيد بينيت الأب (David Bennett Sr.) والذي كان يعاني من مرض قلبي ولم يكن مؤهلاً للحصول على قلب بالطريقة الاعتيادية. لكن بعد 40 يوماً من العملية، مرض بينيت وتوفي بسبب الفشل القلبي.
وضعت هذه التجارب أسس التجارب السريرية والتجارب القياسية التي من شأنها أن تفسح المجال للاستخدام واسع النطاق للأعضاء المنقولة بين الكائنات الحية. في بداية صيف 2022، قام جرّاحون من معهد زرع الأعضاء في مركز لانغوني الصحي التابع لجامعة نيويورك بزرع قلبين من نوع مستولد بشكل خاص من الخنازير في جسمي مريضين كانا يعانيان من الموت الدماغي. راقب الأطباء العلامات الحيوية للمريضين لمدة 3 أيام، وأخذوا عينات من جسميهما واختبروها بحثاً عن الفيروسات. قدّر فريق جامعة نيويورك في مؤتمر صحفي أقيم في 12 يوليو/تموز 2022 وتم الإعلان فيه عن نتائج الاختبارات أن التجارب السريرية قد تبدأ في أي وقت من الآن حتى عام 2025.
اقرأ أيضاً: بعد قرن من الأبحاث: نجاح أول عملية زرع قلب خنزير في جسم إنسان
لكن قبل البدء بهذه التجارب، يجب على الباحثين أن يجدوا الإجابات عن أسئلة متعلقة بآليات وقاية المرضى من الأمراض التي تنتشر بين الخنازير حصراً. اتضح أن القلب الذي تلقّاه بينيت كان مصاباً بنوع من الفيروسات الهربسيّة التي تصيب الخنازير فقط. يحمل هذا الفيروس اسم الفيروس الخنزيري المضخّم للخلايا، ولم يتمكن الأطباء من كشف وجوده قبل إجراء العملية. وجد تحقيق أجري عن عملية الزرع التجريبية هذه والذي نشر في وقت مبكر من شهر يوليو/تموز 2022 في مجلة نيو إنجلاند الطبيّة أن الفيروس لم يُصب خلايا بينيت. ولا يزال من غير المعروف الدور الذي لعبه الفيروس في وفاة بينيت.
لم يكشف الأطباء وجود أي فيروس في التجارب التي أجرتها جامعة نيويورك على المرضى المصابين بالموت الدماغي. مع ذلك، تسلّط تجربة بينيت الضوء على الأسئلة العلمية والأخلاقية التي تعترض طريق التجارب السريرية الخاصة بعمليات جراحية تتطلب الاحتياط من الفيروسات التي تصيب البشر وتلك التي تصيب الأنواع الأخرى على حد سواء.
الإصابات الفيروسية أثناء عمليات زرع الأعضاء أكثر شيوعاً مما تعتقد
تعتبر الأمراض المعدية من مصادر القلق الرئيسية في مجال نقل الأعضاء بين أفراد النوع الواحد.
يقول جاي فيشمان (Jay Fishman)، مدير قسم أمراض عمليات زرع الأعضاء المعدية في مستشفى ولاية ماساتشوستس العام وباحث رائد في مجال نقل الأعضاء بين الكائنات الحية: “تكون لدينا بضع ساعات فقط لإخراج عضو ما وزرعه في جسم المريض المتلقّي”. لذا، على الرغم من أن فريق عملية الزرع يختبر جسم المتبرّع بحثاً عن أمراض مثل التهاب الكبد، فإن نتائج الاختبارات لا تصدر إلا بعد انتهاء العملية. يضيف فيشمان: “أتلقى كل يوم رسائل البريد الإلكتروني من مختلف أنحاء البلاد تنص على أن نتائج بعض الاختبارات كانت إيجابية بالنسبة لمريض ما”، ما يعني أن هذا المريض سيحتاج للخضوع إلى علاج عدوى محتملة الآن.
تعتبر الأمراض التي قد تكون كامنة في أجسام المتبرعين بالأعضاء أو متلقيها مقلقة بشكل خاص في مجال زرع الأعضاء. ومنها المرض الذي يتسبب فيه الفيروس الخنزيري المضخّم للخلايا وجدري الماء والأمراض التي تتسبب بها الديدان الطفيليّة. نظراً لأن هذه الأمراض لا تكون في حالة انتشار نشط، فقد لا تنتج نتيجة إيجابية في اختبارات البوليميراز المتسلسل التي تجرى للكشف عنها. تقول سابنا ميهتا (Sapna Mehta)، المديرة الطبية لدائرة أمراض عمليات زرع الأعضاء المعدية في جامعة نيويورك: “قد تعيش بعض أنواع الطفيليات في جسمك طيلة حياتك دون أن تعرف بوجودها”. وقد تكون الطريقة الوحيدة لكشف هذه العدوى الكامنة هي اختبار الأنسجة العصبية أو العضلية أو اللمفاوية التي توجد فيها هذه العوامل المُمْرضة.
اقرأ أيضاً: نجاح تغيير فصيلة دم الكلى المتبرع بها يفتح آفاقاً جديدة في زراعة الأعضاء
تقول ميهتا إنه عندما يخضع مرضى عمليات زرع الأعضاء للعلاج القاسي باستخدام الأدوية المثبّطة للمناعة لمنع أجهزتهم المناعية من مهاجمة العضو الجديد، “يمكن أن تنشط الفيروسات وتتسبب في عدوى نشطة”. ويمكن أن تكون العدوى كارثية بالنسبة للأشخاص في طور التعافي من العمليات الجراحية الكبرى أو الأمراض الخطيرة التي تصيب الأعضاء.
لكن نظراً لأن إمدادات الأعضاء المتبرّع بها محدودة للغاية، يقوم الأطباء بإجراء عمليات زرع الأعضاء حتى لو كانت هذه الأعضاء تعود لمرضى مصابين بعدوى ما. تقول أنوما نيلور (Anoma Nellore)، المديرة الطبية المساعدة لدائرة زرع الأعضاء وأمراض نقص المناعة المعدية في جامعة ألاباما في برمنغهام: “نعلم أحياناً أن هناك متبرعين [بالكلى الحية] مصابين بالتهاب الكبد سي، وأن هناك متلقين مستعدّين لتلقّي تلك الأعضاء لأن هذا المرض قابل للعلاج”.
أعضاء الحيوانات قد تحمل الفيروسات أيضاً
قد يقلل نقل الأعضاء بين الكائنات الحية من عدم اليقين المتعلق بوجود الأمراض المعدية في الأعضاء التي يتم التبرّع بها، ولكنه يخلق تساؤلات أخرى أيضاً.
يتم إنتاج الخنازير التي يتم أخذ الأعضاء منها في ثلاث شركات أميركية متخصصة بالتكنولوجيا الحيوية، وهي شركة ريفيفيكور (Revivicor) وإي جينيسيس (eGenesis) وماكانا ثيرابيوتكس (Makana Therapeutics). يتم تعديل هذه الخنازير وراثياً لتشكّل أجسامها خلايا لا تكون مغلّفة بالبروتينات والسكريات التي توجد في أجسام البشر، ما يقلل من خطر رفض الجسم للعضو أو ردات الفعل التحسسيّة. ما لا يقل عن هذا التعديل الوراثي أهمية هو أن هذه الخنازير يتم إنتاجها وتربيتها بطريقة تقلل من خطر انتقال العوامل الممرضة خلال عملية الزرع.
قبل إجراء العملية الجراحية، يكون لدى هذه الشركات ما يكفي من الوقت لفحص الخنازير بحثاً عن الأمراض. تقول ميهتا: “تتلقّى هذه الخنازير اللقاحات وتخضع لعمليات إزالة الديدان وفحوصات المراقبة”، وتضيف: “يتم إجراء بعض هذه [الاختبارات] باستخدام دماء الخنازير، بينما يتم إجراء بعضها الآخر باستخدام البراز أو المسحات الأنفية. يتم فحص عينات البراز باستخدام المجاهر بحثاً عن الطفيليات. وتجرى هذه العملية حتى في الوقت الذي يتم استخراج العضو فيه”.
اقرأ أيضاً: ما الذي يعنيه نجاح علماء في استعادة الوظائف الحيوية لخلايا خنزير بعد موته بالنسبة للطب؟
تجري فرق نقل الأعضاء بين الكائنات أيضاً اختباراتها الخاصة. إذ تقول ميهتا إن فريق جامعة نيويورك يجري اختبارات للكشف عن عدد من فيروسات الخنازير التي قد تكون كامنة. أخذ الباحثون في هذا الفريق ضمن تجربتهم الأحدث عيّنات من أحد الخنازير ومن جسم الشخص المتلقّي قبل إجراء عملية الزرع، وأعادوا تلك العملية كل 24 ساعة خلال هذه الدراسة التي دامت 3 أيام.
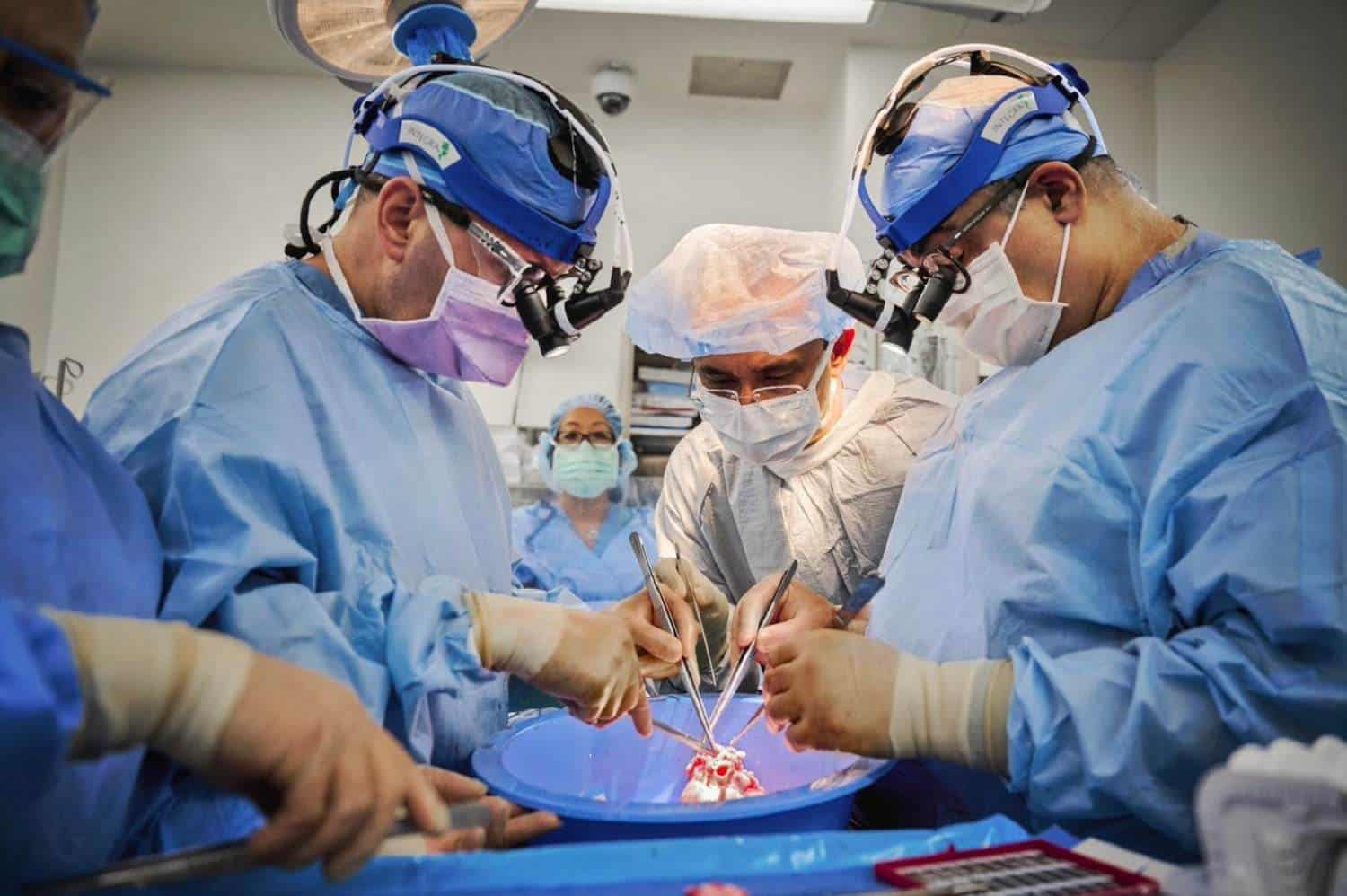
لكن تكنولوجيا وبروتوكولات الاختبارات التي تكشف عن وجود الفيروسات في الخنازير ليست على نفس الدرجة من الموثوقيّة التي تتمتع بها الاختبارات التي تجرى في مجال نقل الأعضاء بين الأفراد من نفس النوع. ويبدو أن هذا هو أحد الأسباب التي أدّت إلى إصابة بينيت. يقول محمّد محيي الدين (Muhammad Mohiuddin)، مدير برنامج نقل الأعضاء القلبية بين الكائنات في جامعة ميريلاند: “كانت نتيجة الاختبار الذي أجري على المسحة الأنفية [بحثاً عن الفيروس الخنزيري المضخّم للخلايا] سلبية”، ويضيف: “لذا بناءً على تجربتنا، كنا متأكدين من أن قلب الخنزير لا يحتوي على هذا الفيروس”.
خلال أول شهرين بعد عملية بينيت الجراحية، بدأ يظهر الفيروس في الاختبارات، وبدأت نسبة مادته الوراثية في دم بينيت بالارتفاع. عندما اختبر فريق الزرع طحال الخنزير مجدداً، وجد الأطباء أن الفيروس موجود وكامن. ويقول محيي الدين: “أصبح السؤال عندها هو ما هو تأثير هذا الفيروس الكامن على جسم بينيت؟”.
اقرأ أيضاً: سبق علمي: الخنزير يصلح رئة الإنسان في جسده ثم يعيدها إليه
بعد وفاة بينيت، اكتشف الجراحون أن الأنسجة في قلبه قد تمزّقت، وأن القلب ككل كان متضخّماً. تشابه هذه الأعراض تلك التي شهدها الباحثون في تجارب نقل الأعضاء بين الخنازير وقرود البابون. وجد الباحثون في هذه التجارب أن القرود التي اتضح أنها مصابة بالفيروس الخنزيري المضخّم للخلايا عاشت لفترة أقصر بـ 3 أسابيع وسطياً بعد الجراحة من القرود غير المصابة بالفيروس.
لكن يقول محيي الدين إنه لم يلحظ أيَّ مؤشرات تبين أن الفيروس كان ينتشر في قلب الخنزير الذي تم زرعه في جسم بينيت. إذ يشرح قائلاً: “لم نرَ الفيروس عندما فحصنا القلب باستخدام المجهر الإلكتروني. وعادة ما يتمكن الأطباء من إيجاد الفيروسات بهذه الطريقة”. قد يكون سبب إيجاد الفريق للفيروس هو إصابة القلب بتلف ناتج عن أسباب أخرى، وقد يكون هذا التلف هو سبب تسرّب الفيروس إلى دم بينيت.
يوافق فيشمان على ذلك، ويقول: “علينا ألا ننسى أن بينيت كان مريضاً للغاية. إذ إنه كان يعاني من العديد من المضاعفات الجراحية، كما أنه كان يستخدم أجهزة دعم الحياة لفترة طويلة من الزمن”، ويضيف: “لم يكن بينيت في الحالة البدينة التي تسمح له بأن يبقى على قيد الحياة، حتى للفترة التي تمكن فيها من ذلك”.
من المحتمل أن الفيروس كان أحد العوامل التي أدّت دوراً محفّزاً في حالة التهابية أكبر أدت في النهاية إلى فشل قلبه. لكن عدم اليقين هذا يسلّط الضوء على قيمة الوقاية من العدوى بغض النظر عن النتائج في مجال البحث العلمي. من الصعب معرفة مدى نجاح عمليات الزرع بوجود عامل إضافي مثل الفيروسات، ما يجعل موازنة مخاطر وفوائد العمليات المستقبلية أكثر صعوبة.
اقرأ أيضاً: نجاح عمل جراحي رائد في إجراء زرع مزدوج لذراعين وكتفين
يقول محيي الدين إن جامعة ميريلاند تخطط لاختبار المزيد من أنسجة الخنازير واستخدام نوع أكثر دقة من اختبارات البوليميراز المتسلسل للكشف عن الفيروس الخنزيري المضخّم للخلايا. على الرغم من أن هذا الاختبار لم ينجح دائماً في الكشف عن العدوى في الدراسات التي أجريت على قرود البابون). يقول محيي الدين إنه بالإضافة لذلك، يجب أن تكون هناك آلية معيارية متفق عليها لعلاج الفيروس الخنزيري المضخّم للخلايا، إذ إنه على الرغم من وجود مضادات فيروسية مخصصة له، فإن آثارها الجانبية كانت أشد بكثير من أن يتحمّلها بينيت.
يقول كل من محيي الدين وفيشمان إن الطريقة الأنسب لضمان أمان الأعضاء المنقولة بين الكائنات تدعى الفحص المصليّ، والتي تكشف وجود الأجسام المضادة للفيروس الخنزيري المضخّم للخلايا في الخنازير التي تؤخذ الأعضاء منها. يكشف هذا الاختبار ما إذا تعرّضت الخنازير إلى أحد العوامل الممرضة في الماضي بدلاً من الكشف عن العدوى الموجودة حالياً. إذا احتوى جسم الخنزير على الأجسام المضادة لعامل ممرض معين، فهذا يعني أنه قد تعرّض من قبل لهذا العامل الممرض وأنه من المحتمل أن الخنزير يأوي عدوى كامنة.
يقول كل من محيي الدين وميهتا إنه حسب معلوماتهما، هذه الاختبارات المعتمدة على الأجسام المضادة يتم إجراؤها حالياً. مع ذلك، قال متحدّث رسمي باسم شركة ريفيفيكور (وهي الشركة التي قامت بتربية كل الخنازير التي استخدمت في الدراسات التي أجريت في 2022) لموقع بوبيولار ساينس (Popular Science) إن الشركة لن تقدّم تصريحات متعلقة بالآليات التي تستخدمها.
اقرأ أيضاً: كيف يمكن للحيوانات أن تساعدنا على فهم الفيروسات؟
أحد التحدّيات الأخرى طويلة الأمد هو وجود أمراض تنتشر بين الخنازير لا يعلم أطباء الزرع كيفية كشفها. تقول ميهتا: “كشفت أغلبية الأبحاث حول الفيروسات التي تصيب الخنازير سلوك هذه الفيروسات في أجسام الخنازير التي تتمتع بأجهزة مناعية صحيّة”. وقد تتصرف بعض هذه الفيروسات بطريقة مختلفة للغاية في جسم إنسان مثبَّط الجهاز المناعي.
تتضمّن مقاربة جامعة نيويورك إجراء الاختبارات التي تكشف وجود فئات كاملة من العوامل الممرضة بدلاً من البحث عن عامل واحد. يقول فيشمان، والذي يدعم استخدام هذه الاختبارات واسعة النطاق: “تساعدنا هذه الاختبارات في كشف وجود أي عوامل ممرضة محتملة”.
حتى الآن، يقول الباحثون في جامعة نيويورك إنهم لم يكتشفوا أي نوع جديد من العوامل الممرضة. إذ تقول ميهتا: “تتضمن أولوياتنا محاولة كشف العوامل الممرضة المعروفة وغير المعروفة”. لكن حالياً، العوامل الممرضة المعروفة هي التي تتسبب بالمشكلات الصحية.
التجارب السريرية قد تكون الخطوة التالية في مجال نقل الأعضاء بين الكائنات
يتفق الأطباء على أن أحد أهم الدروس التي تعلمناها من عملية بينيت هي أننا بحاجة لتطبيق آلية موحّدة لإجراء الاختبارات. تقول ميهتا: “لا يوجد مختبر مركزي يمكننا إرسال العينات إليه”. حالياً، تتضمن التجارب الأربع التي تجرى في الولايات المتحدة مرضى جدد واختبارات مختلفة ومجموعة متنوعة من العلاجات، ما يجعل مقارنة النتائج أمراً صعباً.
على الرغم من ذلك، يشعر فيشمان بالتفاؤل حيال جهوزية مجال نقل الأعضاء بين الكائنات للبدء بالتجارب السريرية. ويقول إن فرق زرع الأعضاء ستمتلك الأدوات المناسبة للتعامل مع العوامل الممرضة المعروفة من خلال تطوير آليات الاختبار والعلاج. يقول فيشمان أيضاً إنه بدون إجراء التجارب السريرية، “لن نتمكن إلّا من تخمين” المخاطر، ويضيف: “نحن نتوخى الحذر، ولكننا نخمّن لا أكثر”.
اقرأ أيضاً: إنجاز نوعي قد يلغي استخدام الأدوية المثبطة للمناعة بعد زرع الأعضاء
لكن تخلق الفيروسات وحالات العدوى غير المعروفة تحدّياً أخلاقياً للتجارب السريرية. إذ إن الحصول على موافقة مستنيرة من المرضى الذين لا يعلمون جميع المخاطر المحتملة لعملية زرع عضو مأخوذ من كائن آخر هو أمر صعب، وخصوصاً “لأنهم لن يتمكّنوا من التخلّص من عواقب المشاركة في تجربة سريرية بعد بدئها”، حسب تعبير نيلور.
